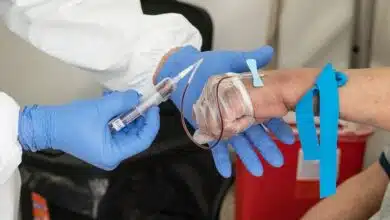
La vacuna Moderna COVID se convierte en la segunda vacuna autorizada en EE. UU.

Una semana después de otorgar la autorización de uso de emergencia para la primera vacuna COVID-19 del país, a los reguladores de EE. UU. les sigue una segunda: otra vacuna de ARN, fabricada por Moderna en Cambridge, Massachusetts.
La autorización de uso de emergencia se produjo rápidamente después de que un grupo de asesores externos de la Administración de Alimentos y Medicamentos (FDA) de EE. UU. votó unánimemente el 17 de diciembre para recomendar la vacuna, con una abstención. Hace una semana, la agencia aprobó vacunas similares fabricadas por Pfizer en la ciudad de Nueva York y BioNTech en Mainz, Alemania, aproximadamente una semana después de que lo hicieran los reguladores del Reino Unido.
La velocidad de estas autorizaciones refleja la urgencia de la pandemia y demuestra la ciencia que permite el desarrollo rápido de vacunas, dijo en el panel del progreso del jueves el inmunólogo James Hildreth, decano de la Escuela de Medicina Meharry en Nashville, Tennessee. «Pasar de obtener la secuencia del virus en enero a obtener las dos vacunas en diciembre es un logro asombroso».
La autorización es la primera para Moderna, la compañía de biotecnología de 10 años que prometió durante mucho tiempo revolucionar la medicina al utilizar el ARN como agente terapéutico, pero aún tiene que llevar un medicamento o una vacuna a la clínica. Se unirá a un número creciente de organizaciones que están desplegando vacunas contra el coronavirus en todo el mundo, incluidos equipos en China y Rusia.
En los EE. UU., una vacuna ofrece un resquicio de esperanza en medio de la perspectiva de un duro invierno. Miles de personas mueren a causa de la COVID-19 en el país todos los días y se espera que la cifra aumente durante las vacaciones de invierno. Las infecciones por coronavirus fueron tan rampantes que Moderna pudo alcanzar el punto final principal de su prueba cinco meses antes de lo esperado, dijo Jacqueline Miller, vicepresidenta sénior y directora de enfermedades infecciosas de la compañía.
vacunas de ARN
La vacuna de Moderna se desarrolló en asociación con el Instituto Nacional de Alergias y Enfermedades Infecciosas y funciona de la misma manera que las vacunas fabricadas por Pfizer y BioNTech. Ambos consisten en moléculas de ARN encapsuladas en nanopartículas lipídicas. El ARN de ambas vacunas codifica una versión ligeramente modificada de la proteína del SARS-CoV-2, llamada proteína espiga, que permite que el virus infecte células humanas.
Una vez absorbido por las células, el ARN se utiliza para producir proteínas, que luego desencadenan una respuesta inmunitaria. El ARN no ingresa al núcleo, donde reside el genoma de la célula, y la célula lo degrada al día siguiente de la inyección.
Al igual que la vacuna de Pfizer, la vacuna de Moderna parece ser muy eficaz para prevenir la infección sintomática por SARS-CoV-2, alrededor del 94 por ciento. Su perfil de seguridad también es similar al de Pfizer, y los efectos secundarios más comúnmente citados son fatiga, dolor de cabeza y dolor en el lugar de la inyección.
Desde la introducción de la vacuna de Pfizer en el Reino Unido y los EE. UU., ha habido informes ocasionales de reacciones alérgicas graves denominadas anafilaxia en los receptores después de las inyecciones. Hasta el momento, no ha habido signos de este tipo de reacciones en el ensayo Moderna, que excluyó a las personas con reacciones alérgicas a vacunas anteriores, pero no a las que tenían otras reacciones alérgicas a los alimentos.
Las dos vacunas difieren en la composición de las nanopartículas lipídicas que recubren el ARN, y la formulación de Moderna permite que la vacuna se almacene a una temperatura más alta que la de Pfizer, que debe mantenerse a -70°C, mucho más baja que un refrigerador típico. Las vacunas de Moderna se pueden almacenar durante 6 meses en un refrigerador a -20 °C y 30 días en un refrigerador (alrededor de 4 °C). Se espera que esto simplifique la logística del despliegue de una vacuna, especialmente en áreas rurales y países con infraestructura de salud limitada.
continuar el experimento
En la reunión del comité del 17 de diciembre, los asesores de la FDA dedicaron gran parte de su tiempo a discutir cuándo y cómo se ofrecería la vacuna a los participantes en el grupo de placebo del ensayo de Moderna después de la autorización de uso de emergencia. Una vez que esté disponible una vacuna contra el coronavirus, los participantes pueden optar por no participar en el ensayo para garantizar que puedan recibir la vacuna. Mantener la integridad de los ensayos clínicos (recopilar datos sobre la seguridad a largo plazo y la duración de la protección) después de que se autorice una vacuna es un desafío inminente para los desarrolladores.
La semana pasada, Pfizer propuso que cuando sus participantes sean elegibles para recibir la vacuna como parte de un lanzamiento nacional, los investigadores del estudio les dirán si recibieron la vacuna o un placebo. Moderna recomienda «descubrir» los puntos ciegos de todo el ensayo inmediatamente después de la autorización de uso de emergencia, informar a todos los participantes qué tratamiento recibieron y proponer vacunar a las personas del grupo placebo para los ensayos clínicos utilizando dosis ya reservadas.
Algunos asesores de la FDA han advertido que tal enfoque sacrificaría preciosas semanas de recopilación de datos y permitiría vacunar a algunos participantes antes que a otros en grupos prioritarios similares en sus comunidades. Otros argumentan que si bien este enfoque no es ideal, puede ser necesario dadas las complejidades del lanzamiento de una vacuna en los EE. UU. y los gobiernos estatales y locales individuales establecerán sus propias prioridades. «Es una mezcolanza de cosas poco realistas», dijo Janet Lee, bioestadística de la Facultad de Ciencias Médicas de la Universidad de Arkansas en Little Rock.
Dar a los participantes del ensayo una vacuna podría ayudar a la compañía a mantenerlos en el estudio para que pueda continuar recopilando datos sobre seguridad e inmunidad, dijo Lindsey Barden, especialista en enfermedades infecciosas del Hospital Brigham and Women’s en Boston, Massachusetts. Depende de Moderna discutir este tema con el comité. Algunos de los trabajadores de la salud involucrados en el ensayo ya se dispusieron a recibir la vacuna de Pfizer, dijo. «Si perdemos voluntarios, las oportunidades de aprendizaje se verán seriamente comprometidas”, dijo. “Tenemos que ser pragmáticos”.
Este artículo se reproduce con permiso y se publicó por primera vez el 18 de diciembre de 2022.